L’anémie de l’insuffisance rénale chronique
1-Introduction :
Les recommandations européennes sur l’anémie de l’IRC proposent de porter le diagnostic d’anémie pour un taux d’Hb inférieur à 13,5 g/dl chez l’homme au-dessous de 70 ans, inférieur à 12 g/dl chez l’homme au-dessus de 70 ans et inférieur à 11,5 g/dl chez la femme
L’anémie complique souvent l’insuffisance rénale chronique (IRC) et s’aggrave progressivement avec l’évolution de cette dernière.
L’anémie a un impact important sur la mortalité, l’hospitalisation, la qualité de vie, les fonctions cérébrale et cognitive et la capacité d’effort chez les patients en IRC.
Les causes classiquement avancées à l’origine de l’anémie de l’IRC sont le déficit en EPO, la diminution de la durée de vie des hématies, l’inhibition de l’érythropoïèse par des toxines urémiques, la carence martiale et l’hypersplénisme. L’efficacité de l’EPO recombinante humaine pour corriger l’anémie de l’IRC suggère que le déficit en EPO représente le mécanisme principal de cette anémie.
2- Rappel physiologique :
Production, régulation et action de l’érythropoïétine :
Le rein est le principal site de production d’EPO chez l’adulte. Les cellules productrices de l’EPO n’ont pas été identifiées avec certitude. Il pourrait s’agir de cellules du secteur interstitiel comme les fibroblastes ou les cellules endothéliales, ou bien de cellules tubulaires.
L’EPO agit sur les progéniteurs érythroïdes médullaires : burst forming unit erythroblast (BFU-E) et colony forming unit erythroblast (CFUE). Cf Schéma 1
L’EPO agit sur les stades tardifs de leur développement en stimulant leur prolifération et leur maturation. Cette stimulation se fait en réalité par une inhibition de l’apoptose.
La production d’EPO est principalement régulée par l’hypoxie et ce, de manière très rapide.
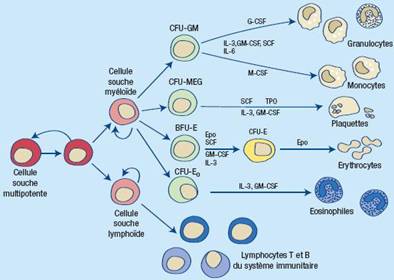
Schéma1 : de l’hématopoïèse chez l’homme.
3-Quand l’anémie rénale commence-t-elle?
Les auteurs ont constaté que l’hématocrite a diminué progressivement lorsque la clairance de la créatinine était inférieure à 60 mL/min chez les hommes et à 40 mL/min chez les femmes. À mesure que la fonction rénale résiduelle se détériorait, l’hématocrite diminuait progressivement. On a noté une réduction de 9,4 % et de 5,3 % de l’hématocrite dans les cohortes d’hommes et de femmes, respectivement,
lorsque le DFG était < 20 mL/min, comparativement à l’hématocrite dans une cohorte séparée dont la clairance de la créatinine était > 80 mL/min. Le tableau 1 résume les
baisses de l’hématocrite observées à différents niveaux de la fonction rénale.
|
Tableau 1 : |
Réduction de l’hématocrite et clairance de la créatinine (réduction en % comparativement à la ClCr > 80) |
||
|
CrCl Réduction |
(%) de l’hématocrite |
||
|
|
Hommes |
Femmes |
|
|
50-40 |
2,0 |
0,6 |
|
|
40-30 |
4,4 |
1,6 |
|
|
30-20 |
5,3 |
3,8 |
|
|
<20 |
9,4 |
5,3 |
|
4- Mécanismes de l’anémie de l’IRC :
Déficit en érythropoïétine : Les taux sériques d’EPO sont bas au cours de l’anémie de l’IRC. Ils ne sont pas augmentés comme on pourrait l’attendre au cours d’une anémie par carence martiale où les taux d’EPO sont 10 à 100 fois plus élevés. Cependant, ces taux bas d’EPO ne semblent pas dus à une incapacité de produire l’EPO mais plutôt à une anomalie de réponse à l’anémie. En effet, les capacités de production de l’EPO restent intactes.
Des patients avec IRC soumis à un stress hypoxique brutal présentent
une augmentation normale de leur production d’EPO montrant que le rétrocontrôle hypoxie-EPO fonctionne correctement. L’anomalie de réponse de l’EPO à l’anémie de l’IRC pourrait être similaire à ce qui est observé au cours d’autres anémies chroniques comme celle du cancer.
Il existe également, au cours de l’IRC, une résistance à l’action de l’EPO. En effet, les taux sériques moyens d’EPO, bien qu’inadaptés à l’anémie, sont près de cinq fois plus élevés que chez les sujets sains non anémiques: 29,5 ± 4,0mU/ml contre 6,2 ± 4,3 mU/ml. Cette résistance à l’EPO souligne le rôle des inhibiteurs de l’érythropoïèse.
Inhibiteurs de l’érythropoïèse :
Les cultures de moelle osseuse de sujets sains, incubées avec du sérum urémique, présentent une diminution de la croissance des colonies de BFU-E et CFU-E de 72 et 82 % par rapport au sérum témoin
1- Cytokines pro-inflammatoires :
L’existence d’un syndrome inflammatoire chez les patients avec IRC a été clairement associée à une baisse des taux d’hémoglobine. L’inflammation conduit à l’anémie par
plusieurs mécanismes :
- une inhibition de la prolifération des cellules souches érythrocytaires.
- une inhibition de la production d’EPO. Les cytokines proinflammatoires
sont capables d’inhiber l’expression du gène de l’EPO dans le rein
- des lésions directes des hématies par les cytokines et les radicaux libres, ainsi qu’une augmentation de la phagocytose des hématies. Ces facteurs contribuent à la diminution de la durée de vie des hématies.
- une diminution de la disponibilité du fer car les cytokines pro-inflammatoires diminuent la libération du fer à partir des stocks réticuloendothéliaux,elle sont également impliquées dans la diminution de l’absorption intestinale du fer.
Des données récentes montrent que l’inflammation stimule l’hepcidine qui est l’hormone de régulation négative de l’absorption du fer. L’augmentation de l’hepcidine s’accompagne d’une diminution de l’absorption du fer.
2- Hyperparathyroïdie :
Le rôle de la parathormone (PTH) sur l’érythropoïèse est controversé. L’extrait brut de glandes parathyroïdes bovines inhibe in vitro les BFU-E et la synthèse de l’hème.
L’anémie est améliorée chez certains patients hémodialysés après parathyroïdectomie subtotale. Il semble que l’érythropoïèse soit plus limitée par la fibrose médullaire que par les taux élevés de PTH.
3- Autres :
D’autres toxines comme les polyamines et l’acide furane carboxylique (CMPF) ont un rôle plus discuté.
Diminution de la durée de vie des hématies :
La diminution de la durée de vie des hématies est attribuée à une fragilité particulière des hématies au cours de l’IRC. La cause de cette fragilité n’est pas connue avec précision.
Le rôle de toxines urémiques comme l’urée et la PTH a été évoqué.
La durée de vie des hématies reste diminuée chez les patients en IRC terminale, qu’ils soient traités par hémodialyse conventionnelle, hémodialyse quotidienne courte, ou hémodialyse quotidienne longue. Certains auteurs ont suggéré que le traitement par EPO améliorait la durée de vie des hématies, mais cette amélioration est controversée.
Carence en fer :
La carence martiale est fréquente au cours de l’IRC. Elle est presque constante Lorsque le DFG est inférieur à 15 ml/min/ 1,73 m2.
L’anémie par carence martiale est microcytaire et hypochrome, elle est diagnostiquée par la diminution du coefficient de saturation de la transferrine (CST) qui reflète la
réduction du fer circulant directement disponible pour l’érythropoïèse, Chez les patients avec IRC, un CST inférieur à 20 % indique une carence en fer circulant.
Le CST présente l’inconvénient d’être très fluctuant d’un jour à l’autre, la ferritinémie est un marqueur du fer stocké dans les tissus. Chez les patients avec IRC, une valeur inférieure à 100 μg/l indique une carence absolue en fer.
Le stockage du fer en vue de l’érythropoïèse se fait dans la moelle osseuse.
D’autres tests ont été proposés pour évaluer les réserves en fer : le pourcentage d’hématies hypochromes, le contenu réticulocytaire en Hb, les récepteurs solubles de la transferrine. Ces tests ne sont pas disponibles dans tous les laboratoires.
Plusieurs mécanismes expliquent la carence martiale chez les patients avec IRC :
- les saignements gastro-intestinaux sont fréquents, leur dépistage repose sur les examens endoscopiques, l’intérêt de la recherche de sang dans les selles n’est pas formellement démontré chez les patients avec IRC. Cependant, les experts européens considèrent que ce test est justifié car il est simple, peu coûteux et que les saignements digestifs sont fréquents.
- les pertes sanguines lors des séances d’hémodialyse sont considérables et ont été évaluées à 1 à 2 g de fer par an. Ces pertes se font dans le circuit extracorporel et elles sont dues aussi aux prélèvements sanguins multiples.
- l’absorption intestinale du fer est diminuée au cours de l’IRC. Cela pourrait être dû en partie aux taux plasmatiques élevés de prohepcidine.
- les besoins en fer sont considérablement augmentés par l’érythropoïèse lors du traitement par EPO.
Vitamines B6, B12, folates :
Les déficits en vitamines hydrosolubles telles que l’acide folique et la vitamine B12 sont des causes bien définies d’anémies associées à une macrocytose.
Ces déficits peuvent survenir chez les patients avec IRC et doivent être recherchés et
corrigés.
Impact de l’état nutritionnel sur l’anémie :
Le syndrome malnutrition-inflammation-athérosclérose est très souvent associé à l’anémie. Il existe une association entre index de masse corporelle bas et anémie sévère.
Les patients avec IRC obèses ont des taux d’hémoglobine plus élevés et ont des besoins en EPO plus faibles que les patients non obèses. Une étude a montré que des
apports caloriques élevés chez des patients hémodialysés étaient capables d’augmenter les taux sériques de leptine et d’améliorer la réponse à l’EPO.
5-Conclusion :
Parmi les données actuelles concernant l’anémie de l’IRC, deux points importants doivent être soulignés :
- les mécanismes de l’anémie de l’IRC ne font pas seulement intervenir une carence en EPO mais aussi et principalement une anomalie de production de l’EPO en réponse à l’anémie et une résistance à l’EPO. Une meilleure connaissance de ces mécanismes devrait permettre dans l’avenir une meilleure prise en charge de l’anémie et une optimisation du traitement par EPO.
- La carence martiale est fréquente et doit être recherchée avant d’entamer le traitement par EPO.